Артериальная гипертензия (АГ) остается одной из наиболее важных медико–социальных проблем и ведущим фактором риска развития инфаркта миокарда и мозгового инсульта [1]. Рост смертности от сердечно–сосудистых заболеваний определяет высокую актуальность проблемы лечения АГ. Среди групп лекарственных препаратов, применяемых для лечения АГ, ши¬роко используются антагонисты кальция (АК). Современные АК обладают высокой антигипертензивной эффективностью и органопротективным действием, имеют хорошую переносимость.
Важное место среди АК занимает амлодипин. Амлодипин представляет собой АК дигидропиридинового ряда III поколения по классификации T. Toya–Oka и W. Nayler [2].
Его характеризуют высокая биодоступность, достигающая 90%, длительный период полувыведения (35–50 ч) и большая продолжительность действия, которая позволяет принимать препарат 1 раз в сутки и контролировать артериальное давление (АД) равномерно в течение суток [3,4]. Амлодипин отличается высокой тканевой селективностью, его эффект на гладкомышечные клетки сосудов в 80 раз превышает воздействие на кардиомиоциты. За счет этого амлодипин вызывает выраженное снижение общего периферического сосудистого сопротивления и практически не влияет на сократимость миокарда, функцию синусового узла и атрио–вентрикулярную проводимость [5]. Амлодипин обладает выраженным гипотензивным действием в отношении как систолического, так и диастолического АД. Результаты проведенных клинических исследований свидетельствуют о высокой антигипертензивной эффективности этого препарата: у пожилых пациентов среднее снижение систолического АД при его применении составило 24,1 мм рт.ст., у больных изолированной систолической АГ – 25,9 мм рт.ст., у больных сахарным диабетом – 19,8 мм рт.ст., у пациентов с хронической почечной недостаточностью – 19,1 мм рт.ст. [6]. Препарат хорошо переносится пациентами, при внезапном прекращении его приема не наблюдается синдрома отмены [3].
В 1992 г. компания Pfizer выпустила амлодипина безилат в таблетированной форме для приема 1 раз в сутки (в России дозировка 5–10 мг), зарегистрировав его под торговыми названиями Норваск. Норваск является одним из самых изученных представителей класса АК. Практически все данные по безопасности и эффективности амлодипина касаются его безилатной соли. За период с 1980 по 2010 г. проведено 800 клинических испытаний амлодипина безилата, в которых участвовало более 600 тыс. пациентов.
К числу наиболее интересных и показательных исследований, в которых участвовал амлодипин безилат, следует отнести ALLHAT, VALUE, PREVENT, CAPARES, CAMELOT. В исследовании ALLHAT проводился сравнительный анализ влияния терапии тремя различными классами препаратов на частоту развития сердечно–сосудистых осложнений у пациентов с АГ. В исследование были включены более 30 тыс. пациентов, период лечения в среднем составил около 5 лет. По влиянию на сердечно–сосудистый прогноз амлодипин оказался сопоставимым с иАПФ лизиноприлом, а по ряду позиций превзошел последний [7]. По данным исследования ALLHAT, амлодипин наиболее эффективно снижал риск общей смертности, частоту возникновения ишемической болезни сердца (ИБС) и ее осложнений. Кроме того, амлодипин превосходил лизиноприл по предупреждению заболеваний периферических сосудов и инсультов [7].
В многоцентровом исследовании VALUE, включавшем более 15 тыс. пациентов АГ, проводилось сравнение эффективности терапии амлодипином и блокатором рецепторов ангиотензина валсартаном [8]. Результаты исследования не обнаружили статистических различий по частоте развития инсультов, инфарктов миокарда и летальности при лечении амлодипином и валсартаном. Гипотензивный эффект (особенно начальный) оказался более выраженным на фоне приема амлодипина. Полученные данные еще раз подчеркивают возможность достижения целевого уровня АД при лечении амлодипином [8].
В свете общепризнанной в наши дни концепции сердечно–сосудистого континуума важным критерием оценки эффективности антигипертензивного препарата являются его органопротективные свойства. В многочисленных экспериментальных и клинических исследованиях была показана способность АК вызывать обратное развитие гипертрофии миокарда левого желудочка (ГЛЖ) [9,10]. Исследование FOAM доказало, что по способности вызывать регресс ГЛЖ амлодипин уступает только иАПФ, превосходя препараты других классов [10].
Многочисленные экспериментальные и клинические исследования свидетельствуют об антиатеросклеротическом эффекте амлодипина, что является важным моментом в лечении больных АГ и ИБС [11–13]. Антиатерогенное действие АК обусловлено их антиоксидантными и антипролиферативными свойствами, что препятствует проникновению и депонированию эфиров холестерина в сосудистой стенке. Амлодипин, как и другие АК, обладает способностью замедлять агрегацию тромбоцитов. В исследовании PREVENT у 825 больных с ангиографическими признаками стенозирующего атеросклероза амлодипин достоверно уменьшал толщину интимы сонных артерий [11]. В двойном слепом плацебо–контролируемом исследовании CAPARES назначение амлодипина больным, перенесшим коронарную ангиопластику, снижало суммарный риск неблагоприятных исходов на 35% [12]. В рамках сравнительного рандомизированного исследования CAMELOT с помощью внутрисосудистой эхо–графии изучено влияние амлодипина на прогрессирование коронарного атеросклероза. У больных ИБС при приеме амлодипина отмечалась достоверная тенденция к снижению прогрессирования атеросклеротического процесса [13].
Высокая востребованность амлодипина объясняет появление на мировом фармацевтическом рынке все большего числа воспроизведенных препаратов (генериков). Их количество исчисляется десятками, однако данные о биоэквивалентности, не говоря уже о терапевтической эквивалентности, практически отсутствуют. Известны случаи, когда воспроизведенные препараты не были биоэквивалентными [14].
Для доказательства эквивалентности генерика оригинальному препарату используют данные фармацевтической эквивалентности, а также данные биоэквивалентности, под которой понимают фармакокинетическую эквивалентность оригинального и воспроизведенного препарата. Исследования биоэквивалентности проводят на ограниченном контингенте здоровых добровольцев с помощью рандомизированного перекрестного метода [15]. В качестве показателей фармакокинетики оценивают максимальную концентрацию препарата (Cmax) и время ее достижения, а также площадь под кривой «концентрация–время», так называемую AUC (area under curve). Считается, что 90% значений AUC препарата–генерика не должны выходить за пределы 80–125% от таких же показателей для оригинального препарата. Если это условие соблюдается, то делается вывод о биоэквивалентности генерика и оригинального препарата [16,17].
Возникает вопрос: может ли терапия препаратами–генериками реально обеспечить тот результат в отношении улучшения прогноза жизни больных, который был доказан в крупных контролируемых исследованиях, использовавших оригинальные препараты? Формальная точка зрения гласит, что если препарат–генерик зарегистрирован (т.е. имеются данные о его фармацевтической и фармакокинетической эквивалентности оригинальному препарату), то он терапевтически эквивалентен оригинальному препарату [15]. Однако многие исследователи высказывают сомнения по поводу того, всегда ли этих данных достаточно, чтобы гарантировать реальную терапевтическую эквивалентность генерика оригинальному препарату.
Помимо оригинального бренда амлодипина безилата, защищенного патентом, во многих странах Европы появились воспроизведенные препараты, содержащие в качестве действующего вещества амлодипина малеат [18,19]. Начиная с 2007 г., во всем мире стали доступны и генерики амлодипина безилата.
Сравнительное изучение биоэквивалентности амлодипина малеата оригинальному препарату проводилось в нескольких исследованиях. Так, в открытом рандомизированном перекрестном исследовании Mignini F. et al. (2007) была изучена биоэквивалентность амлодипина малеата оригинальному препарату амлодипина безилат у 24 здоровых добровольцев (возраст 24–45 лет) [20]. Исследователи не обнаружили никакой статистически достоверной разницы между этими веществами по показателям AUC и Cmax, был сделан вывод о биоэквивалентности амлодипина малеата и амлодипина безилата.
В работе Abernethy D.R. et al. (1990) было показано, что с возрастом фармакокинетика амлодипина меняется, поэтому исследования по оценке биоэквивалентности амлодипина необходимо проводить в группе пациентов пожилого возраста [21].
Эффективность и безопасность амлодипина бези¬лата и амлодипина малеата изучалась в многоцентровом рандомизированном клиническом исследовании Park S. еt al., проведенном в 2005 г. в Южной Корее [22]. В исследовании участвовали 118 пациентов с АГ, которые были рандомизованы в две группы. Пациенты первой группы для лечения АГ принимали амлодипина безилат, больные второй группы получали амлодипина малеат. Оценка результатов исследования проводилась через 8 недель лечения по предварительно заданному критерию – изменению уровня диастолического АД более чем на 4 мм рт.ст. Согласно данному критерию оценки в группе амлодипина малеата динамика снижения диастолического АД была такой же, как и в группе амлодипина безилата. Разница снижения диастолического АД не была статистически значимой. Авторы сделали вывод, что эффективность амлодипина малеата сопоставима с антигипертензивным эффектом амлодипина безилата [22].
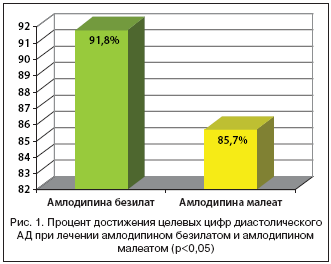
Однако при детальном анализе этого исследования было установлено, что достижение целевых значений диастолического АД наблюдалось у 91,8% больных при приеме амлодипина безилата и только у 85,7% пациентов, получавших амлодипин малеат [22] (рис. 1). Кроме того, выбор величины изменения диастолического АД был произвольным. В мета–анализе Wald D.S. et al. (2009) было доказано, что изменение диастолического АД на 4 мм рт.ст. обусловливает разницу по частоте развития ИБС на 20%, а мозгового инсульта на 29% [23]. В таком случае нивелирование разницы диастолического АД в пределах 4 мм рт.ст. является грубым нарушением в оценке полученных данных и делает сомнительным статистическую достоверность полученных результатов исследования.
Получается, что не стоит говорить о том, что эти лекарства взаимозаменяемы, так как исследования были ограничены малой численностью выборки и отсутствием отдаленных результатов наблюдения [14]. Чтобы говорить о терапевтической эквивалентности препаратов с точки зрения их антигипертензивного действия необходимы испытания в когортах численностью не менее 600 человек, продолжительностью наблюдения не менее 6 мес., с оценкой конечных точек исследования (числа инфарктов миокарда, мозгового инсульта и общая летальность). Наилучшей оценкой при изучении терапевтической эквивалентности оригинального и воспроизведенного препарата является проведение крупномасштабных продолжительных рандомизированных клинических исследований [14].
Таким образом, амлодипина безилат является единственным хорошо изученным препаратом амлодипина с доказанным в крупных многоцентровых международных исследованиях антигипертензивным эффектом, органопротективными свойствами и хорошим профилем переносимости, что гарантирует достижение цели лечения пациентов.
Литература
1. ESH–ESC Guidelines Committee. 2007 guidelines for the management of arterial hypertension.// J Hypertension 2007; 25: 1105–87.
2. Toyo–Oka T, Nayler WG. Third generation calcium entry blockers. Blood Press 1996; 5: 206–208.
3. Nold G. et al. Morning versus evening amlodipine treatment: Effect of circadian blood pressure profile in essential hypertensive patients. Blood Press Monit 1998 3(1) 17–25.
4. Leenen F.H. et al. Persistence of antihypertensive effect after missed doses of calcium antagonist with long (amlodipine) vs short (diltiazem) elimination half–life. British J Clin Pharmacol 1996 41(2) 83–8.
5. Clavijo GA, de Clavijo IV, Weart CW. Amlodipine: a new calcium antagonist. Am J Hosp Pharm 1994; 51: 59–68.
6. Levine CB, Fahrbach KR, Frame D, et al. Effect of amlodipine on systolic blood pressure. Clin Therapeutics 2003;25:35–57.
7. Leenen FH, Nwachuku CE, Black HR et al. Clinical events in high–risk hypertensive patients randomly assigned to calcium channel blocker versus angiotensin–converting enzyme inhibitor in the antihypertensive and lipid–lowering treatment to prevent heart attack trial. Hypertension 2006; 48: 374–84.
8. Julius S, Kjeldsen SE, Weber M et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipin: the VALUE randomized trial. Lancet 2004; 363 (9426): 2022–3.
9. Liebson P.R., Grandits G.A., Dianzumba S. et al. Comparison of five antihypertensive monotherapies and placebo for change in left ventricular mass in patients receiving nutritional–hygienic therapy in the Treatment of Mild Hypertension Study (TOMHS) // Circulation 1995; 91: 698–706.
10. Zanchetti A, Ruilope LM, Cuspidi C, Macca G, Verschuren J, Kerselaers W. Comparative effects of the ACE inhibitor fosinopril and the calcium antagonist amlodipine on left ventricular hypertrophy and urinary albumin excretion in hypertensive patients. Results of FOAM, a multicenter European study.// J Hypertens, 2001; 19(Suppl 2):S92.
11. Hernandez RH, Armas–Hernandez MJ, Velasco M. Calcium antagonists and atherosclerosis protection in hypertension.// Am J Ther., 2003; 10(6):409–14.
12. Jоrgensen B, Thaulow E; Effects of amlodipine on ischemia after percutaneous transluminal coronary angioplasty: secondary results of the Coronary Angioplasty Amlodipine Restenosis (CAPARES) Study.//Am Heart J., 2003;145(6):1030–5.
13. Nissen SE, Tuzcu EM, Libby P, Thompson PD, Ghali M, Garza D, Berman L, Shi H, Buebendorf E, Topol EJ, CAMELOT Investigators. Effect of antihypertensive agents on cardiorprovascular events in patients with coronary disease and normal blood pressure: the CAMELOT study: a randomized controlled trial. // JAMA, 2004; 292:2217–2225.
14. Meredith P.A. Potential concerns about generic substitution: bioequivalence versus therapeutic equivalence of different amlodipine salt forms.//Current Medical Research and Opinion, 2009; 25: 2179–2189.
15. Марцевич С.Ю., Кутишенко Н.П., Деев А.Д, Оригинальные препараты и дженерики в кардиологии. Можно ли решить проблему взаимозаменяемости? // Вестник Росздравнадзора, 2009, №4 стр. 5–8.
16. Senn S. In the blood: proposed new requirements for registering generic drugs. // Lancet 1998;352:85–86.
17. Meyer G.F. History and regulatory issues of generic drugs. // Transplantation Proceedings 1999;31 (Suppl. 3A):10S–12S.
18. European Medicines Agency (EMEA), Committee for Proprietary Medicinal Products (CPMP), Opinion following an article 29 referral: Amlovita. London 26 April 2004. EMEA/CPMP/539/04.
19. European Medicines Agency (EMEA), Committee for Proprietary Medicinal Products (CPMP), Opinion following an article 29 referral: Talam. London 27 April 2004. EMEA/CPMP/540/04.
20. Mignini F, Tomassoni D, Traini E, et al. Single–dose, randomized, crossover bioequivalence study of amlodipine maleate versus amlodipine besylate in healthy volunteers. // Clin Exp Hypertens 2007;29:539–52.
21. Abernethy DR, Gutkowska J, Winterbottom LM. Effects of amlodipine, a long–acting dihydropyridine calcium antagonist in aging hypertension: pharmacodynamics in relation to disposition. //Clin Pharmacol Ther 1990;48:76–86.
22. Park S, Chung N, Kwon J, et al. Results of a multicenter, 8–week, parallel–group, randomized, double–blind, doubledummy, phase III clinical trial to evaluate the efficacy and tolerability of amlodipine maleate versus amlodipine besylate in Korean patients with mild to moderate hypertension. //Clin Ther 2005;27:441–50.
23. Wald DS, Law M, Morris JK, et al. Combination therapy versus monotherapy in reducing blood pressure: meta–analysis on 11,000 participants from 42 trials. // Am J Med 2009;122:290–300.
Подзолков В.И., Тарзиманова А.И.

 Опубликовано в категории:
Опубликовано в категории:  Метки:
Метки: